GB4789.12-2016 肉毒梭菌及肉毒素检验
发布时间:2024-06-28 浏览次数:1454 分享:
肉毒梭菌检验的卫生学意义
产生的神经麻痹毒素(肉毒毒素),可引起人和动物中毒,依据其毒素不同,将其分为7种不同的型
分类 | 可引起中毒的肉毒梭菌型 |
引起人群中毒 | A、B、E、F(只发生于丹麦与美国) |
引起畜、禽中毒 | C(α、β)、D |
未知 | G |
A、B型分布最广,土壤,水底均有发现,C、D多存在于动物尸体,E多存在于海洋沉积物中(菌体与芽孢均适应于深水低温)
临床:常见于豆谷类的发酵食品,如臭豆腐,豆瓣酱,豆豉等。腊肉,香肠等熏制食品发现的较少。
潜伏期(与摄入毒素量,毒力和个体的状态有关)
国外报到多为12-36h
国内最短6h,最长60h
症状与体征(主要症状都是神经麻痹的表现)
非特异性的刺激:头晕,头疼,恶心;甚至呕吐,腹泻
肉毒特有症状:视力减弱,全身无力,语言困难,呼吸困难(直接死因),但神志清醒
由于其生长特性,家庭制的发酵食品比较容易成为肉毒梭菌的产生环境。
肉毒梭菌的生物学特性
形态与染色:
▶ 厌氧性杆状菌,新鲜培养的革兰氏为阳性,多形态性细菌(直杆状/稍弯曲)。4~8根周生鞭毛,行动迟缓,没有荚膜。
▶ 形成芽孢,芽孢比繁殖体宽,卵圆形,位于次级端,或偶位于中央,常见游离芽孢。
培养特性:
▶ 固体培养基上形成3mm左右,非正圆形,表面颗粒状,边缘不整齐,界限不明显、绒毛网状,向外扩散。
▶ 厌氧。
▶ 生长温度25-35°C,生长pH 6.0~8.2。
▶ 卵黄平板上有乳浊环,表面有彩虹薄层。
▶ 卵黄平板上有乳浊环,表面有彩虹薄层。肉毒梭菌的生化性状很不规律,即使同型,也常常见到株间差异。
肉毒毒素:
肉毒毒素的毒性极强,是最强的神经麻痹毒素之一,1克毒素能杀死400万吨小白鼠,一个人的致死量不会大于2微克。但需要注意的是不同物种对不同毒素的敏感性不同。
肉毒毒素为外毒素,有文献表明其毒素由菌体表面产生,在菌体成熟或崩解后释放于环境中。
本身为大分子蛋白,引起人群中毒的A,B,E三种都可分为两个蛋白成分:一个具有神经毒性,一个为无毒性的血凝素。、
部分肉毒毒素有被激活的性质:在肠道中被胰酶激活,导致毒性大幅度提升(常见于E型毒素)
对许多理化作用是比较不稳定的
耐热:A型60℃,2分钟加热,差不多完全破坏,B,E,二型要70℃ 2分钟加热才能完全破坏,而C型需要90℃ 2分钟D型需要70℃40分钟。
pH:耐酸而不耐碱。
肉毒梭菌及肉毒毒素检验
一个是毒素检出(更为重要,只有检出有毒素,才能做出肯定性结论),一个是细菌鉴定。(时间较长,延误治疗时机)
患者血清是最好的检样,但要获得可供做出诊断的血清,需要看中毒的程度如何和采血的时间是否合适。
食剩的可疑食品
不得已的情况下,也可采用患者呕吐物或者胃液。
肉毒梭菌及肉毒毒素检验程序
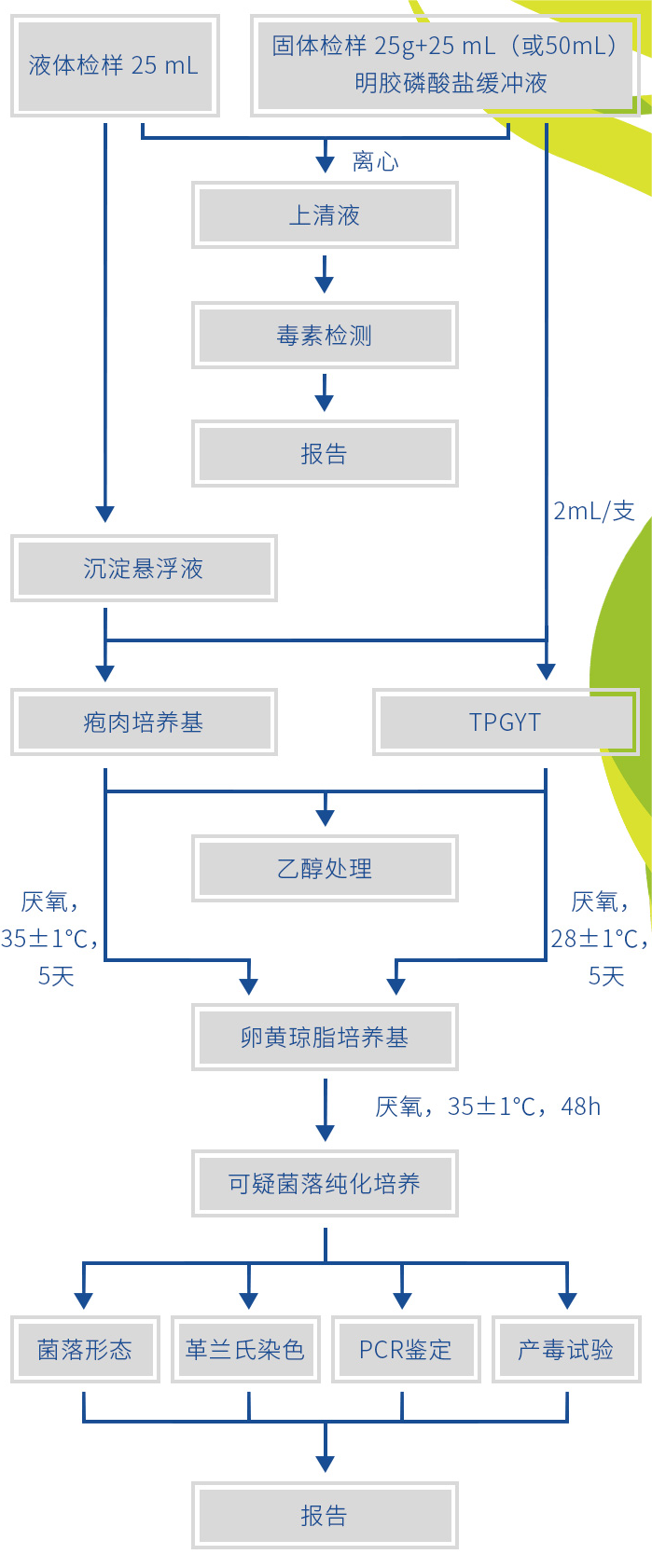
1、增菌培养
◆ 5.3.1 增菌培养与检出试验
◆ 5.3.1.1 取出庖肉培养基4支和TPGY 肉汤管2支,隔水煮沸10min~15min,排除溶解氧,迅速冷却,切勿摇动,在TPGY 肉汤管中缓慢加入胰酶液至液体石蜡液面下肉汤中,每支1 mL,制备成TPGYT。
◆ 5.3.1.2 吸取样品匀液或毒素制备过程中的离心沉淀悬浮液2mL接种至庖肉培养基中,每份样品接种4支,2支直接放置35℃±1℃厌氧培养至5d,另2支放80℃保温10min,再放置35℃±1℃厌氧培养至5d;同样方法接种2支TPGYT肉汤管,28℃±1℃厌氧培养至5d。
◆ 注:接种时,用无菌吸管轻轻吸取样品匀液或离心沉淀悬浮液,将吸管口小心插入肉汤管底部,缓缓放出样液至肉汤中,切勿搅动或吹气。
5.3.1.3 检查记录增菌培养物的浊度、产气、肉渣颗粒消化情况,并注意气味。肉毒梭菌培养物为产气、肉汤浑浊(庖肉培养基中A 型和B型肉毒梭菌肉汤变黑)、消化或不消化肉粒、有异臭味。
5.3.1.4 取增菌培养物进行革兰氏染色镜检,观察菌体形态,注意是否有芽胞、芽胞的相对比例、芽胞在细胞内的位置。
5.3.1.5 若增菌培养物5d无菌生长,应延长培养至10d,观察生长情况。
5.3.1.6 取增菌培养物阳性管的上清液,按5.2方法进行毒素检出和确证试验,必要时进行定型试验,阳性结果可证明样品中有肉毒梭菌存在。
注:TPGYT增菌液的毒素试验无需添加胰酶处理。
2、分离培养
◆ 5.3.2.1 增菌液前处理,吸取1mL增菌液至无菌螺旋帽试管中,加入等体积过滤除菌的无水乙醇,混匀,在室温下放置1h。
◆ 5.3.2.2 取增菌培养物和经乙醇处理的增菌液分别划线接种至卵黄琼脂平板,35 ℃±1 ℃厌氧培养48h。
◆ 5.3.2.3 观察平板培养物菌落形态,肉毒梭菌菌落隆起或扁平、光滑或粗糙,易成蔓延生长,边缘不规则,在菌落周围形成乳色沉淀晕圈(E型较宽,A 型和B型较窄),在斜视光下观察,菌落表面呈现珍珠样虹彩,这种光泽区可随蔓延生长扩散到不规则边缘区外的晕圈。
◆ 5.3.2.4 菌株纯化培养,在分离培养平板上选择5个肉毒梭菌可疑菌落,分别接种卵黄琼脂平板,35℃±1℃,厌氧培养48h,按5.3.2.3观察菌落形态及其纯度。
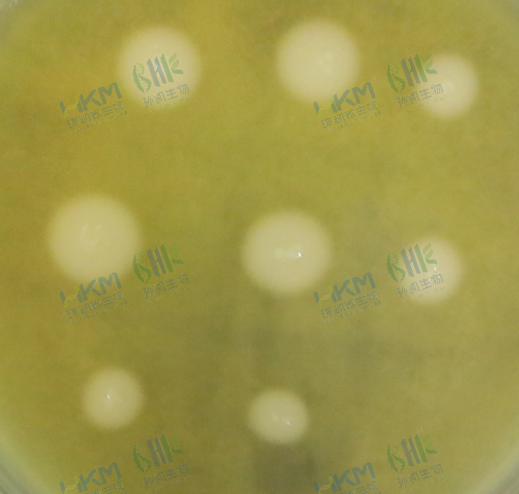
梭状芽孢杆菌在卵黄琼脂上形态
3、鉴定实验
◆ 5.3.3 鉴定实验
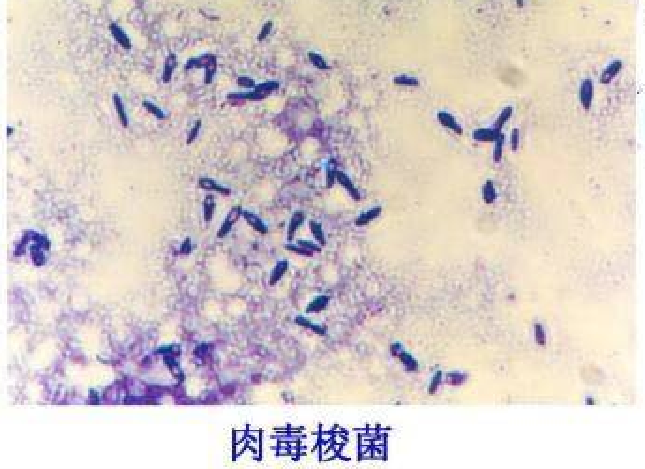
◆ 5.3.3.1 染色镜检
挑取可疑菌落进行涂片、革兰氏染色和镜检,肉毒梭菌菌体形态为革兰氏阳性粗大杆菌、芽胞卵圆形、大于菌体、位于次端,菌体呈网球拍状。
◆ 5.3.3.2 毒素基因检测
4、毒素基因检测
a)菌株活化:挑取可疑菌落或待鉴定菌株接种TPGY,35℃±1℃厌氧培养24h。
b)DNA 模板制备:
◆ 吸取TPGY培养液1.4 mL至无菌离心管中,
◆ 14000×g 离心2 min,弃上清,
◆ 加入1.0 mL BS悬浮菌体,
◆ 14000×g 离心2 min,弃上清,
◆ 用400μL PBS重悬沉淀,
◆ 加入10 mg/mL 溶菌酶溶液100 μL,摇匀,37 ℃水浴15 min,
◆ 加入10 mg/mL 蛋白酶K 溶液10 μL,摇匀,60 ℃水浴1h,再沸水浴10 min,
◆ 14000×g 离心2 min,上清液转移至无菌小离心管中,
◆ 加入3 mol/L NaAc溶液50 μL和95%乙醇1.0 mL,摇匀,-70 ℃ 或 -20 ℃ 放置30 min,
◆ 14000×g 离心10 min,弃去上清液,
◆ 沉淀干燥后溶于200 μL TE缓冲液,置于-20 ℃保存备用。
◆ 注:根据实验室实际情况,也可采用常规水煮沸法或商品化试剂盒制备DNA模板。
c)核酸浓度测定(必要时):
◆ 取5μLDNA 模板溶液,加超纯水稀释至1mL,
◆ 用核酸蛋白分析仪或紫外分光光度计分别检测 260nm 和 280nm 波段的吸光值A260和A280。按式(1)计算DNA浓度。
◆ 当浓度在0.34μg/mL—340μg/mL或A260/A280比值在1.7—1.9之间时,适宜于PCR扩增。
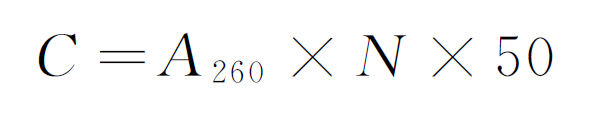
C ——— DNA 浓度,单位为微克每毫升(μg/mL);
A260 —— 260nm 处的吸光值;
N ——— 核酸稀释倍数。
d)PCR扩增:
1) 分别采用针对各型肉毒梭菌毒素基因设计的特异性引物(见表1)进行PCR扩增,包括
● A型肉毒毒素(botulinumneurotoxinA,bont/A)、
● B型肉毒毒素(botulinumneurotoxinB,bont/B)、
● E型肉毒毒素(botulinumneurotoxinE,bont/E)、
● F型肉毒毒素(botulinumneurotoxinF,bont/F)
每个PCR反应管检测一种型别的肉毒梭菌。

2) 反应体系配制见表2,反应体系中各试剂的量可根据具体情况或不同的反应总体积进行相应调整。

3) 反应程序,预变性95℃、5min;循环参数94℃、1min,60℃、1min,72℃、1min;循环数40;后延伸72℃,10min;4℃保存备用。
4) PCR扩增体系应设置阳性对照、阴性对照和空白对照。用含有已知肉毒梭菌菌株或含肉毒毒素基因的质控品作阳性对照、非肉毒梭菌基因组DNA 作阴性对照、无菌水作空白对照。
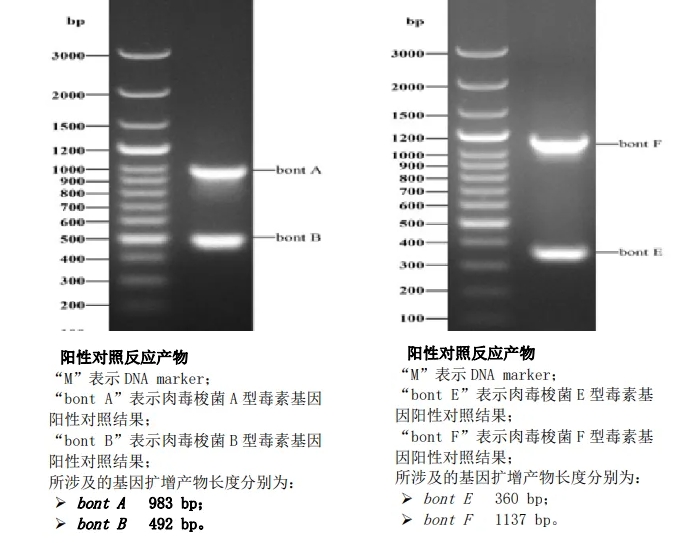
e)凝胶电泳检测PCR扩增产物:
◆ 用0.5×TBE缓冲液配制1.2%—1.5%的琼脂糖凝胶,凝胶加热融化后冷却至60℃左右加入溴化乙锭至0.5μg/mL或Goldview5μL/100mL制备胶块,
◆ 取10μL PCR扩增产物与2.0μL 6×加样缓冲液混合,点样,其中一孔加入DNA 分子量标准。0.5×TBE电泳缓冲液,10V/cm 恒压电泳。
◆ 根据溴酚蓝的移动位置确定电泳时间,用紫外检测仪或凝胶成像系统观察和记录结果。
PCR扩增产物也可采用毛细管电泳仪进行检测。
f)结果判定:
◆ 阴性对照和空白对照均未出现条带,阳性对照出现预期大小的扩增条带(见表1),判定本次PCR检测成立;
◆ 待测样品出现预期大小的扩增条带,判定为PCR结果阳性,根据表1判定肉毒梭菌菌株型别,待测样品未出现预期大小的扩增条带,判定PCR结果为阴性。
注:PCR试验环境条件和过程控制应参照GB/T27403《实验室质量控制规范 食品分子生物学检测》规定执行。
肉毒梭菌 E/ F 型毒素基因PCR 检测试剂盒(KJD07P)
▶ 产品组成:
组分名称 | 规格×数量 |
冻干试剂 | 8 管 × 3 排 |
复溶液 | 1 mL × 1 管 |
阳性对照 | 1管(冻干型) |
阴性对照 | 1管(冻干型) |
裂解液 | 1 mL × 1 管 |
超纯水 | 1 mL × 1 管 |
6 × Loading buffer | 240 μL × 1 管 |
说明书 | 1份 |
◆ 5.3.3.3 菌株产毒试验
● 将PCR阳性菌株或可疑肉毒梭菌菌株接种庖肉培养基或TPGYT 肉汤(用于E型肉毒梭菌),按5.3.1.2条件厌氧培养5d,按5.2方法进行毒素检测和(或)定型试验,毒素确证试验阳性者,判定为肉毒梭菌,根据定型试验结果判定肉毒梭菌型别。
● 注:根据PCR阳性菌株型别,可直接用相应型别的肉毒毒素诊断血清进行确证试验。
4、毒素检测
◆ 5.2.1毒素液制备
取样品匀液约40mL或均匀液体样品25mL放入离心管,3000 r/min离心10min~20min,收集上清液分为两份放入无菌试管中,一份直接用于毒素检测,一份用于胰酶处理后进行毒素检测。液体样品保留底部沉淀及液体约12mL,重悬,制备沉淀悬浮液备用。
胰酶处理:用1mol/L氢氧化钠或1mol/L盐酸调节上清液pH 至6.2,按9份上清液加1份10%胰酶(活力1∶250)水溶液,混匀,37℃孵育60min,期间间或轻轻摇动反应液。
◆ 5.2.2检出试验
用5号针头注射器分别取离心上清液和胰酶处理上清液腹腔注射小鼠3只,每只0.5mL,观察和记录小鼠48h内的中毒表现。典型肉毒毒素中毒症状多在24h内出现,通常在6h内发病和死亡,其主要表现为竖毛、四肢瘫软,呼吸困难,呈现风箱式呼吸、腰腹部凹陷、宛如峰腰,多因呼吸衰竭而死亡,可初步判定为肉毒毒素所致。若小鼠在24h后发病或死亡,应仔细观察小鼠症状,必要时浓缩上清液重复试验,以排除肉毒毒素中毒。若小鼠出现猝死(30min内)导致症状不明显时,应将毒素上清液进行适当稀释,重复试验。
注:毒素检测动物试验应遵循GB15193.2《食品安全国家标准 食品毒理学实验室操作规范》的规定。
◆ 5.2.3确证试验
上清液或(和)胰酶处理上清液的毒素试验阳性者,取相应试验液3份,每份0.5mL,其中
● 第一份加等量多型混合肉毒毒素诊断血清,混匀,37℃孵育30min;
● 第二份加等量明胶磷酸盐缓冲液,混匀后煮沸10min;
● 第三份加等量明胶磷酸盐缓冲液,混匀。
将三份混合液分别腹腔注射小鼠各两只,每只0.5mL,观察96h内小鼠的中毒和死亡情况。
结果判定:若注射第一份和第二份混合液的小鼠未死亡,而第三份混合液小鼠发病死亡,并出现肉毒毒素中毒的特有症状,则判定检测样品中检出肉毒毒素。
结论 | 状况分类 |
肉毒毒素 | 第一份和第二份未死亡,第三份死亡,并出现肉毒毒素中毒的特有症状, |
有其他易热性毒素,也可能是肉毒毒力过强,需要稀释 | 第一份死亡,第二份未死亡,第三份死亡 |
细菌性外毒素以外的毒素或毒物 | 第一份,第二份,第三份都死亡 |
无毒素,或稀释过度 | 都未死亡 |
结果报告
◆ 6.1肉毒毒素检测结果报告
● 根据5.2.2和5.2.3试验结果,报告25g(mL)样品中检出或未检出肉毒毒素。
● 根据5.2.5定型试验结果,报告25g(mL)样品中检出某型肉毒毒素。
◆ 6.2肉毒梭菌检验结果报告
● 根据5.3各项试验结果,报告样品中检出或未检出肉毒梭菌或检出某型肉毒梭菌。







